Das Funktionsprinzip des Zirkoniumdioxid-O2-Sensors misst den Sauerstoffpartialdruck in einem Gasgemisch. Dies führt in der Regel zu Verwirrung bei den Kunden von PST, da die meisten Sauerstoffsensoren auf dem Markt die Sauerstoffkonzentration messen.
Aber was ist Partialdruck? Diese Frage wird uns häufig gestellt, wenn es um das Funktionsprinzip des O2-Sensors geht. In diesem Artikel befassen wir uns mit der Definition des Partialdrucks, der Physik dahinter, wie man den Partialdruck berechnet und wie man den Sauerstoffpartialdruck in einen Volumengehalt umrechnet, für diejenigen, die sich für die Sauerstoffkonzentration interessieren.
Partialdruck: Die Definition
Der Partialdruck ist definiert als der Druck einer einzelnen Gaskomponente in einem Gasgemisch. Er entspricht dem Gesamtdruck, den die einzelne Gaskomponente ausüben würde, wenn sie allein das gesamte Volumen einnehmen würde.
Daltons Gesetz: Die Physik
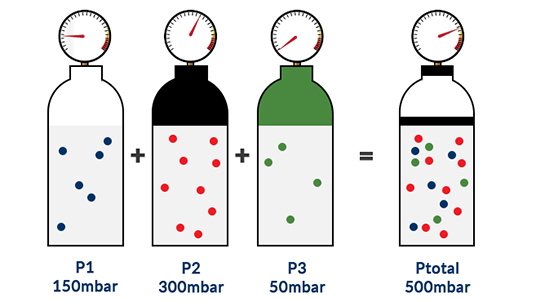
Die Theorie des Funktionsprinzips des O2-Sensors wird hier ausführlich erläutert. Der Gesamtdruck (Ptotal) eines Gemischs idealer Gase entspricht der Summe der Partialdrücke (Pi) der einzelnen Gase in diesem Gemisch.
| k |
| i=1 |
| ni |
| ntotal |
| Pi |
| Ptotal |
| ni | Anzahl der Partikel im Gas |
| ntotal | Gesamtzahl der Partikel |
| pi | Partialdruck des Gases i |
| Ptotal | Gesamtdruck |
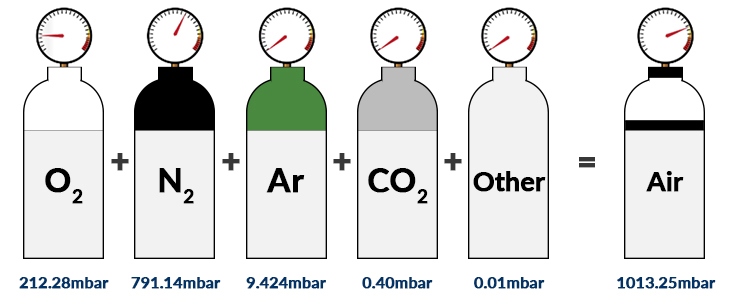
Beispiel 1:
Der atmosphärische Druck auf Meereshöhe (unter Standard-Atmosphärenbedingungen) beträgt 1013,25 mbar. Die Hauptbestandteile trockener Luft sind hier Stickstoff (78,08 Vol.-%), Sauerstoff (20,95 Vol.-%), Argon (0,93 Vol.-%) und Kohlendioxid (0,040 Vol.-%). Der Volumenanteil (%) kann mit der Anzahl der Teilchen (n) gleichgesetzt werden, da die oben genannten Gase als ideale Gase angenähert werden können.
Gleichung 2 kann nach dem Partialdruck eines einzelnen Gases (i) aufgelöst werden, um Folgendes zu erhalten:
| ni |
| ntotal |
| 20.95% |
| 100% |
Dieser Wert ist natürlich nur bei trockener Atmosphäre (0 % Luftfeuchtigkeit) relevant. Bei Feuchtigkeit wird ein Teil des Gesamtdrucks durch den Wasserdampfdruck verursacht. Daher kann der Sauerstoffpartialdruck (ppO₂) genauer berechnet werden, wenn neben dem barometrischen Gesamtdruck auch die relative Luftfeuchtigkeit und die Umgebungstemperatur gemessen werden.
Zunächst wird der Wasserdampfdruck berechnet:
| HRel |
| 100 |
| WVP | Wasserdampfdruck(mbar) |
| HRel | relative Luftfeuchtigkeit (%) |
| WVPmax | Maximaler Wasserdampfdruck (mbar) |
Bei bekannter Umgebungstemperatur kann der maximale Wasserdampfdruck (WDDmax) anhand der nachstehenden Tabelle bestimmt werden. Der maximale Wasserdampfdruck wird auch als Taupunkt bezeichnet. Warme Luft kann mehr Wasserdampf aufnehmen und hat daher einen höheren WDDmax.
| Temperatur (°C) | Max. Wasserdampf Druck (mbar) | Temperatur (°C) | Max. Wasserdampf Druck (mbar) |
| 0 | 6.1 | 31 | 44.92 |
| 1 | 6.57 | 32 | 47.54 |
| 2 | 7.06 | 33 | 50.3 |
| 3 | 7.58 | 34 | 53.19 |
| 4 | 8.13 | 35 | 56.23 |
| 5 | 8.72 | 36 | 59.42 |
| 6 | 9.35 | 37 | 62.76 |
| 7 | 10.01 | 38 | 66.27 |
| 8 | 10.72 | 39 | 69.93 |
| 9 | 11.47 | 40 | 73.77 |
| 10 | 12.27 | 42.5 | 84.19 |
| 11 | 13.12 | 45 | 95.85 |
| 12 | 14.02 | 47.5 | 108.86 |
| 13 | 14.97 | 50 | 123.86 |
| 14 | 15.98 | 52.5 | 139.5 |
| 15 | 17.04 | 55 | 457.42 |
| 16 | 18.17 | 57.5 | 177.25 |
| 17 | 19.37 | 60 | 199.17 |
| 18 | 20.63 | 62.5 | 223.36 |
| 19 | 21.96 | 65 | 250.01 |
| 20 | 23.37 | 67.5 | 279.31 |
| 21 | 24.86 | 70 | 311.48 |
| 22 | 26.43 | 75 | 385.21 |
| 23 | 28.11 | 80 | 473.3 |
| 24 | 29.82 | 85 | 577.69 |
| 25 | 31.66 | 90 | 700.73 |
| 26 | 33.6 | 95 | 844.98 |
| 27 | 35.64 | 100 | 1013.17 |
| 28 | 37.78 | 110 | 1433.61 |
| 29 | 40.04 | 120 | 1988.84 |
| 30 | 42.42 | 130 | 2709.58 |
Der Sauerstoffpartialdruck entspricht dann:
| 20.95 |
| 100 |
| ppO2 | Sauerstoffpartialdruck O2 (mbar) |
| BP | Luftdruck (mbar) |
| WVP | Wasserdampfdruck (mbar) |
Beispiel 2 unten beschreibt die Auswirkung von Feuchtigkeit auf die Reduzierung des Sauerstoffpartialdrucks und damit auf den Volumengehalt von Sauerstoff.
Beispiel 2:
An einem typischen Tag werden die folgenden Informationen von einer kalibrierten Wetterstation aufgezeichnet:
| Temperatur | 22°C |
| Feuchtigkeit | 32% |
| Luftdruck | 986mbar |
Unter Verwendung der obigen Tabelle zur Ermittlung des Wasserdampfdrucks ergibt sich ein maximaler Wasserdampfdruck von 26,43 mbar.
| 32 |
| 100 |
Der Sauerstoffpartialdruck entspricht dann:
| 20.95 |
| 100 |
Da wir nun den Sauerstoffpartialdruck und den barometrischen Gesamtdruck kennen, können wir den volumetrischen Sauerstoffgehalt berechnen.
| 204.8 |
| 986 |

