O princípio de funcionamento do sensor de O2 de dióxido de zircônio mede a pressão parcial de oxigênio em uma mistura de gases. Isso normalmente causa confusão entre os clientes da PST, pois a maioria dos sensores de oxigênio no mercado mede a concentração de oxigênio.
Mas o que é pressão parcial? Essa é uma pergunta que nos fazem com frequência quando se trata do princípio de funcionamento do sensor de O2. Neste artigo, abordaremos a definição de pressão parcial, a física por trás dela, como calcular a pressão parcial e como converter a pressão parcial de oxigênio em conteúdo volumétrico para os interessados na concentração de oxigênio.
Pressão parcial: a definição
A pressão parcial é definida como a pressão de um único componente de gás em uma mistura de gases. Ela corresponde à pressão total que o componente de gás único exerceria se ocupasse sozinho todo o volume.
Lei de Daltons: A Física
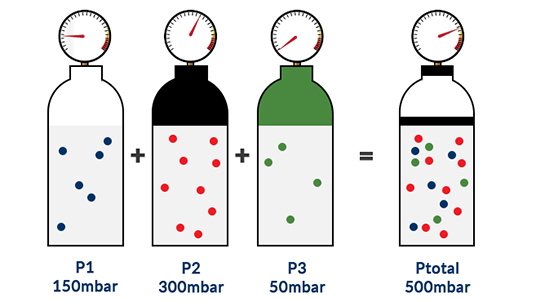
A teoria do princípio de funcionamento do sensor de o2 está detalhada aqui. A pressão total (Ptotal) de uma mistura de gases ideais é igual à soma das pressões parciais (Pi) dos gases individuais nessa mistura.
| k |
| i=1 |
| ni |
| ntotal |
| Pi |
| Ptotal |
| ni | Número de partículas no gás |
| ntotal | Número total de partículas |
| pi | Pressão parcial do gás i |
| Ptotal | Pressão total |
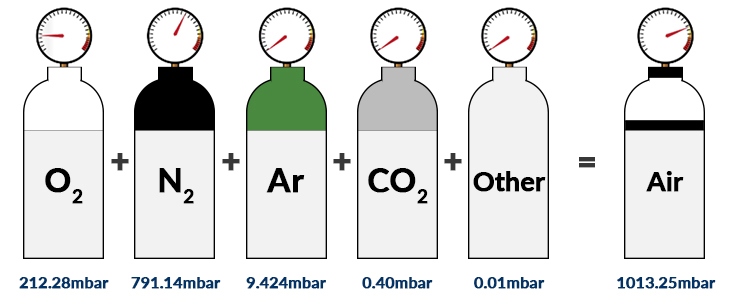
Exemplo 1:
A pressão atmosférica no nível do mar (sob condições atmosféricas padrão) é de 1013,25mbar. Aqui, os principais componentes do ar seco são nitrogênio (78,08% Vol.), oxigênio (20,95% Vol.), argônio (0,93% Vol.) e dióxido de carbono (0,040% Vol.). O conteúdo volumétrico (%) pode ser igualado ao número de partículas (n), já que os gases acima podem ser aproximados como gases ideais.
A Equação 2 pode ser resolvida para a pressão parcial de um gás individual (i) para obter:
| ni |
| ntotal |
| 20.95% |
| 100% |
É claro que esse valor só é relevante quando a atmosfera está seca (0% de umidade). Se houver umidade, uma proporção da pressão total é absorvida pela pressão do vapor de água. Portanto, a pressão parcial de oxigênio (ppO₂) pode ser calculada com mais precisão quando a umidade relativa e a temperatura ambiente são medidas junto com a pressão barométrica total.
Em primeiro lugar, a pressão do vapor de água é calculada:
| HRel |
| 100 |
| WVP | Pressão de vapor de água (mbar) |
| HRel | Umidade relativa (%) |
| WVPmax | Pressão máxima de vapor de água (mbar) |
Para uma temperatura ambiente conhecida, a pressão máxima de vapor de água (WVPmax) pode ser determinada na tabela de pesquisa abaixo. A pressão máxima de vapor de água também é chamada de ponto de orvalho. O ar mais quente pode reter mais vapor de água e, portanto, tem um WVPmax mais alto.
| Temperatura (°C) | Vapor máximo de água Pressão (mbar) | Temperatura (°C) | Vapor máximo de água pressão (mbar) |
| 0 | 6.1 | 31 | 44.92 |
| 1 | 6.57 | 32 | 47.54 |
| 2 | 7.06 | 33 | 50.3 |
| 3 | 7.58 | 34 | 53.19 |
| 4 | 8.13 | 35 | 56.23 |
| 5 | 8.72 | 36 | 59.42 |
| 6 | 9.35 | 37 | 62.76 |
| 7 | 10.01 | 38 | 66.27 |
| 8 | 10.72 | 39 | 69.93 |
| 9 | 11.47 | 40 | 73.77 |
| 10 | 12.27 | 42.5 | 84.19 |
| 11 | 13.12 | 45 | 95.85 |
| 12 | 14.02 | 47.5 | 108.86 |
| 13 | 14.97 | 50 | 123.86 |
| 14 | 15.98 | 52.5 | 139.5 |
| 15 | 17.04 | 55 | 457.42 |
| 16 | 18.17 | 57.5 | 177.25 |
| 17 | 19.37 | 60 | 199.17 |
| 18 | 20.63 | 62.5 | 223.36 |
| 19 | 21.96 | 65 | 250.01 |
| 20 | 23.37 | 67.5 | 279.31 |
| 21 | 24.86 | 70 | 311.48 |
| 22 | 26.43 | 75 | 385.21 |
| 23 | 28.11 | 80 | 473.3 |
| 24 | 29.82 | 85 | 577.69 |
| 25 | 31.66 | 90 | 700.73 |
| 26 | 33.6 | 95 | 844.98 |
| 27 | 35.64 | 100 | 1013.17 |
| 28 | 37.78 | 110 | 1433.61 |
| 29 | 40.04 | 120 | 1988.84 |
| 30 | 42.42 | 130 | 2709.58 |
Partial oxygen pressure then equates to:
| 20.95 |
| 100 |
| ppO2 | Pressão parcial de O2 (mbar) |
| BP | Pressão barométrica (mbar) |
| WVP | Pressão de vapor da água (mbar) |
O exemplo 2 abaixo descreve o efeito da umidade que reduz a pressão parcial de oxigênio e, portanto, o conteúdo volumétrico de oxigênio.
Exemplo 2:
Em um dia normal, as seguintes informações são registradas em uma estação meteorológica calibrada:
| temperatura | 22°C |
| umidade | 32% |
| Pressão barométrica | 986mbar |
Usando a tabela de consulta de pressão de vapor de água acima, WVPmax = 26,43mbar.
| 32 |
| 100 |
A pressão parcial de oxigênio equivale a:
| 20.95 |
| 100 |
Como agora sabemos a pressão parcial de oxigênio e a pressão barométrica total, podemos calcular o conteúdo volumétrico de oxigênio.
| 204.8 |
| 986 |
Quer ver mais informações como esta?
Inscreva-se em um de nossos boletins informativos do setor e receba nossas notícias e insights relacionados mais recentes diretamente em sua caixa de entrada!
Sign Up
