
Comment la technologie de surveillance en temps réel de la TSP joue un rôle essentiel dans l'intégrité, la qualité et la sécurité des données
La gestion efficace des données est essentielle au succès de presque toutes les entreprises. Pour les entreprises de production pharmaceutique en particulier, la collecte, l'organisation, l'analyse et l'utilisation des données provenant de l'ensemble du cycle de production sont essentielles.
La gestion des données est essentielle pour un certain nombre de raisons :
- Optimisation des processus : Une modélisation robuste des données permet aux fabricants d'identifier les domaines à améliorer, de rationaliser les processus et d'optimiser les ressources, améliorant ainsi la productivité et réduisant les coûts.
- Cohérence d'un lot à l'autre : Quelle que soit l'échelle de fabrication, la constance de la production est un critère essentiel pour garantir une qualité de produit uniforme et donc des résultats thérapeutiques prévisibles pour les patients.
- Amélioration continue : L'analyse continue des données provenant de l'ensemble de l'infrastructure de production permet aux fabricants de produits pharmaceutiques d'identifier les tendances et les problèmes potentiels, et de mettre en œuvre des mesures préventives ou d'affiner les processus.
- Contrôle de la qualité : Une gestion précise et complète des données est un aspect essentiel du contrôle de la qualité et du respect de la production correcte et des spécifications du produit.
- Conformité réglementaire : En fin de compte, l'intégrité et la traçabilité des données sont cruciales pour démontrer que chaque étape du processus de production pharmaceutique, de la recherche et du développement au point de livraison, répond aux normes réglementaires les plus élevées afin de protéger la sécurité des consommateurs et la réputation des entreprises.
Gestion des données et BPF
La gestion des données est également fondamentale pour que les fabricants de produits pharmaceutiques puissent se conformer aux exigences des bonnes pratiques de fabrication (BPF). L'Organisation mondiale de la santé définit les BPF comme "un système garantissant que les produits sont fabriqués et contrôlés de manière cohérente, conformément aux normes de qualité. Elles sont conçues pour minimiser les risques liés à la production pharmaceutique qui ne peuvent être éliminés en testant le produit final. ... Les BPF couvrent tous les aspects de la production : depuis les matériaux de départ, les locaux et les équipements jusqu'à la formation et l'hygiène personnelle du personnel. Des procédures écrites et détaillées sont essentielles pour chaque processus susceptible d'affecter la qualité du produit fini. Des systèmes doivent être mis en place pour prouver, documents à l'appui, que les procédures correctes sont suivies de manière cohérente à chaque étape du processus de fabrication - à chaque fois qu'un produit est fabriqué'.
Il est clair qu'aucun de ces objectifs ne peut être atteint sans de solides procédures de collecte, d'analyse et d'interprétation des données, puis d'utilisation des informations obtenues pour le contrôle et l'optimisation de la production en temps réel, ainsi que pour l'établissement de rapports et le respect de la réglementation.
Gestion des données pour les applications GxP
La bonne nouvelle, c'est que l'explosion récente des technologies numériques, portée par des initiatives telles que Industry 4.0 et son équivalent pour la fabrication de produits pharmaceutiques, Pharma 4.0, en cours de développement par l'Agence européenne pour la sécurité des médicaments (ESA), a permis d'améliorer la qualité de vie des patients. Société internationale d'ingénierie pharmaceutique, apporte à l'industrie une nouvelle génération de systèmes avancés et intelligents. Ces technologies offrent aux ingénieurs et aux responsables du développement, de la production, de la qualité et de la chaîne d'approvisionnement des possibilités passionnantes d'atteindre de nouveaux sommets en matière de productivité, de qualité des produits, de traçabilité et de respect des réglementations.
À la tête de ce mouvement se trouvent des solutions telles que notre Système de surveillance en temps réel (RMS). Cette plateforme innovante combine GAMP5 category 4 software with hardware catégorie 1 et exploite la puissance de la technologie numérique pour aider les fabricants à se concentrer sur les défis clés de la saisie et de l'intégrité des données.
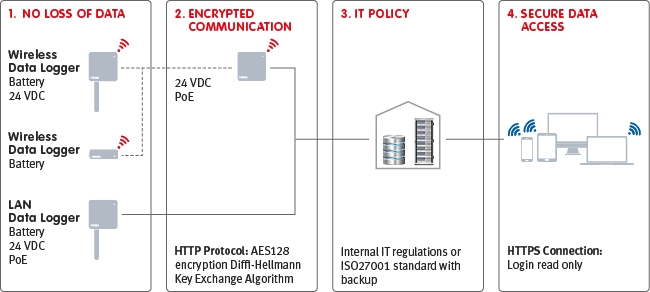
Une solution RMS intègre généralement un réseau de capteurs, de sondes et d'enregistreurs de données avec ou sans fil, connectés à une base de données et à une plateforme logicielle d'analyse sur site ou dans un nuage sécurisé. Cela permet, par exemple, de mesurer la température, l'humidité relative, la pression différentielle ou les concentrations de gaz, les données de chaque appareil étant automatiquement capturées par le logiciel du système. Ce dernier fournit ensuite une série de fonctionnalités, notamment un accès à plusieurs niveaux, des tableaux de bord utilisateur personnalisables, une surveillance à distance en temps réel avec des alarmes et des alertes interactives, ainsi que la génération automatique de rapports et de scripts de validation.
La plateforme RMS est facile à installer et à configurer, et elle est conforme à EudraLex Annexe 11 de l'UE et FDA CFR 21 Part 11, ce qui en fait un outil idéal pour tous les processus GxP, y compris les BPL, les BPF et les BPD. Sa conception modulaire facilite sa mise à l'échelle, ce qui lui permet d'être déployé dans une seule zone de traitement, telle qu'une salle blanche, puis, une fois le concept éprouvé, d'être étendu à l'ensemble de l'infrastructure de production.
Quelle que soit la nature ou l'ampleur de la mise en œuvre, la technologie RMS fournit aux fabricants de produits pharmaceutiques une multitude de données de haute intégrité sur lesquelles ils peuvent s'appuyer. Associée à une puissante plateforme de surveillance et d'analyse, elle crée de nouvelles opportunités pour améliorer l'optimisation des processus, l'utilisation, la qualité, la cohérence et, surtout, la conformité aux réglementations.
Découvrez comment notre système de surveillance modulaire Rotronic peut améliorer la fabrication de produits pharmaceutiques.

Related Information
La surveillance de l'environnement est essentielle pour les processus BPF
BMS, EMS et GMP dans la production pharmaceutique
Vue d'ensemble du système de surveillance Rotronic
Blogs associés
Données, contrôle des processus et responsabilité pour la fabrication de produits pharmaceutiques sous contrat
Pourquoi le système de surveillance en temps réel PST convient-il à votre laboratoire ?
Vue d'ensemble du système de surveillance Rotronic
Importance de la mesure de l'humidité dans les chambres climatiques
Mesure de l'activité de l'eau dans l'industrie pharmaceutique
Comment mesurer l'activité de l'eau dans la fabrication de produits pharmaceutiques
Catégories associées
Produits apparentés
Système de surveillance continue Rotronic RMS
Logger de données - Rotronic RMS T30-868
Loggers de données - Rotronic RMS-LOG-T30-L
RMS-LOG-L-D - Logger de données avec affichage
Capteur Numérique de Température - Rotronic RMS-TCD-S-001
Capteurs de Pression Différentielle - Rotronic RMS PCD-S
Capteurs d'humidité et de température - Rotronic RMS-HCD-S
Loggers de données - Interface LAN - Rotronic RMS-LOG-L
Enregistreur de données - Interface sans fil - 868 MHZ - Rotronic RMS-LOG-868
Gateway - Rotronic RMS-GW-868
Vous voulez voir plus d'informations comme celle-ci ?
Inscrivez-vous à l'une de nos lettres d'information sur l'industrie et vous recevrez directement dans votre boîte aux lettres électronique nos dernières informations et réflexions sur le sujet !
S'inscrire
