El principio de funcionamiento del sensor de O₂ de dióxido de circonio consiste en medir la presión parcial del oxígeno en una mezcla de gases. Esto suele generar confusión entre los clientes de PST, ya que la mayoría de los sensores de oxígeno del mercado miden la concentración de oxígeno.
Pero, ¿qué es la presión parcial? Es una pregunta que nos hacen con frecuencia cuando se trata del principio de funcionamiento del sensor de O2. En este artículo, abordaremos la definición de presión parcial, la física que hay detrás, cómo se calcula la presión parcial y cómo convertir la presión parcial de oxígeno en contenido volumétrico para aquellos interesados en la concentración de oxígeno.
Presión parcial: la definición
La presión parcial se define como la presión de un único componente gaseoso en una mezcla de gases. Corresponde a la presión total que ejercería ese único componente gaseoso si ocupara por sí solo todo el volumen.
La ley de Dalton: la física
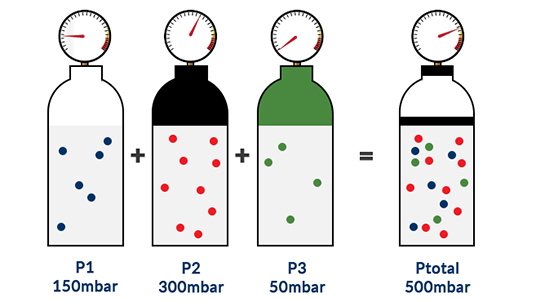
La teoría del principio de funcionamiento del sensor de O2 se detalla aquí. La presión total (Ptotal) de una mezcla de gases ideales es igual a la suma de las presiones parciales (Pi) de los gases individuales de dicha mezcla.
| k |
| i=1 |
| ntotal |
| Pi |
| Ptotal |
| ni | Número de partículas en el gas |
| ntotal | Número total de partículas |
| pi | Presión parcial del gas i |
| Ptotal | Presión total |
Ejemplo 1:
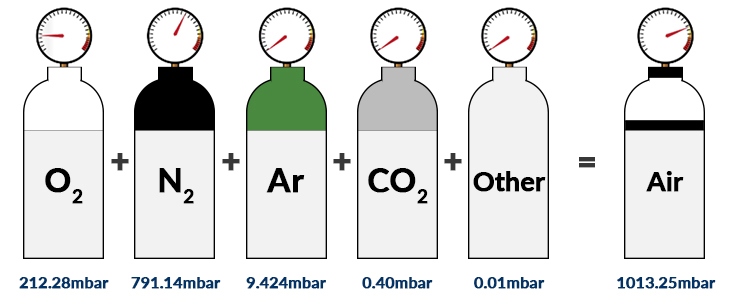
La presión atmosférica al nivel del mar (en condiciones atmosféricas estándar) es de 1013,25 mbar. En este caso, los principales componentes del aire seco son el nitrógeno (78,08 % vol.), el oxígeno (20,95 % vol.), el argón (0,93 % vol.) y el dióxido de carbono (0,040 % vol.). El contenido volumétrico (%) puede equipararse al número de partículas (n), ya que los gases mencionados pueden aproximarse como gases ideales.
La ecuación 2 puede resolverse para la presión parcial de un gas individual (i) y se obtiene:
| ni |
| ntotal |
| 20,95 % |
| 100 % |
Por supuesto, este valor solo es relevante cuando la atmósfera está seca (0 % de humedad). Si hay humedad presente, una parte de la presión total corresponde a la presión del vapor de agua. Por lo tanto, la presión parcial de oxígeno (ppO₂) se puede calcular con mayor precisión cuando se miden la humedad relativa y la temperatura ambiente junto con la presión barométrica total.
En primer lugar, se calcula la presión del vapor de agua:
| HRel |
| 100 |
| WVP | Presión de vapor de agua (mbar) |
| HRel | Humedad relativa (%) |
| WVPmax | Presión máxima de vapor de agua (mbar) |
Para una temperatura ambiente conocida, la presión máxima de vapor de agua (WVPmax) puede determinarse a partir de la tabla de consulta que figura a continuación. La presión máxima de vapor de agua también se conoce como punto de rocío. El aire más cálido puede contener más vapor de agua y, por lo tanto, tiene una WVPmax más alta.
| Temperatura (°C) | Presión máxima de vapor de agua (mbar) | Temperatura (°C) | Presión máxima de vapor de agua (mbar) |
| 0 | 6,1 | 31 | 44,92 |
| 1 | 6,57 | 32 | 47,54 |
| 2 | 7,06 | 33 | 50,3 |
| 3 | 7,58 | 34 | 53,19 |
| 4 | 8,13 | 35 | 56,23 |
| 5 | 8,72 | 36 | 59,42 |
| 6 | 9,35 | 37 | 62,76 |
| 7 | 10,01 | 38 | 66,27 |
| 8 | 10,72 | 39 | 69,93 |
| 9 | 11,47 | 40 | 73,77 |
| 10 | 12,27 | 42,5 | 84,19 |
| 11 | 13,12 | 45 | 95,85 |
| 12 | 14,02 | 47,5 | 108,86 |
| 13 | 14,97 | 50 | 123,86 |
| 14 | 15,98 | 52,5 | 139,5 |
| 15 | 17,04 | 55 | 457,42 |
| 16 | 18,17 | 57,5 | 177,25 |
| 17 | 19,37 | 60 | 199,17 |
| 18 | 20,63 | 62,5 | 223,36 |
| 19 | 21,96 | 65 | 250,01 |
| 20 | 23,37 | 67,5 | 279,31 |
| 21 | 24,86 | 70 | 311,48 |
| 22 | 26,43 | 75 | 385,21 |
| 23 | 28,11 | 80 | 473,3 |
| 24 | 29,82 | 85 | 577,69 |
| 25 | 31,66 | 90 | 700,73 |
| 26 | 33,6 | 95 | 844,98 |
| 27 | 35,64 | 100 | 1013,17 |
| 28 | 37,78 | 110 | 1433,61 |
| 29 | 40,04 | 120 | 1988,84 |
| 30 | 42,42 | 130 | 2709,58 |
La presión parcial de oxígeno se calcula entonces como:
| 20,95 |
| 100 |
| ppO2 | Presión parcial de O2 (mbar) |
| BP | Presión barométrica (mbar) |
| WVP | Presión del vapor de agua (mbar) |
El ejemplo 2 que figura a continuación describe el efecto de la humedad en la reducción de la presión parcial de oxígeno y, por lo tanto, del contenido volumétrico de oxígeno.
Ejemplo 2:
En un día típico, se registra la siguiente información procedente de una estación meteorológica calibrada:
| Temperatura | 22 °C |
| Humedad | 32 % |
| Presión barométrica | 986 mbar |
Utilizando la tabla de consulta de presión de vapor de agua anterior, WVPmáx = 26,43 mbar.
| 32 |
| 100 |
La presión parcial de oxígeno se calcula entonces como:
| 20,95 |
| 100 |
Ahora que conocemos la presión parcial de oxígeno y la presión barométrica total, podemos calcular el contenido volumétrico de oxígeno.
| 204,8 |
| 986 |
Quiere ver más información como ésta?
Suscríbase a uno de nuestros boletines del sector y recibirá directamente en su bandeja de entrada nuestras noticias y opiniones más recientes.
Inscribirse
